原子の大小関係
問 次の原子の大小関係を答えよ。
⑴ リチウム原子とナトリウム原子
⑵ ナトリウム原子とマグネシウム原子
原子の大きさに関する問題だね。
うーん、こんなの覚えていないと無理なんじゃないですか?
原子の大きさを正確に答えるなんて、専門家でも難しいよ。比較できるかが問題なんだ。
それぞれの原子の構造を図示してごらん。
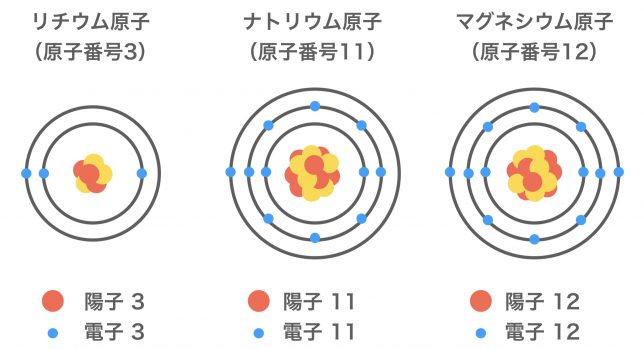
こうなりますね。
同族での比較
これをみて、⑴の問題は分からないかい?
リチウムとナトリウムでは、電子殻がひとまわり大きいナトリウムの方が、原子の大きさは大きくなりそうですね。
それでいいよ。
一般に、周期表の周期が大きくなればなるほど、最外殻が増えるぶん原子が大きくなるよ。
リチウムとナトリウムは同じ1族の元素。
ナトリウムは第3周期、カリウムは第4周期だから、カリウムの方が大きいと考えればいいのですね。
その通り。
同じ族では下の方が大きい。と覚えておこう。ちなみに実際の原子は、ナトリウム原子の半径が0.186nm(ナノメートル)でカリウム原子の半径が0.227nmくらいだよ。
同周期での比較
じゃあ、⑵の問題はどうなりますか?
ナトリウムもマグネシウムも同じ第3周期ですよ。
そうだね。
同じ周期の場合は、原子核に存在する陽子の数がポイントとなる。
陽子の数ですか?
ナトリウムは11個、マグネシウムは12個ですね。
陽子は正の電荷をもつ粒子だ。
陽子の数が多ければ多いほど、中心の原子核のプラスの力が強くなる。つまり、負の電荷をもつ電子を強く引きつけるんだ。
マグネシウムの方が原子核の正の電荷が少し大きくて、より電子を中心に引きつけていると考えるわけですね。
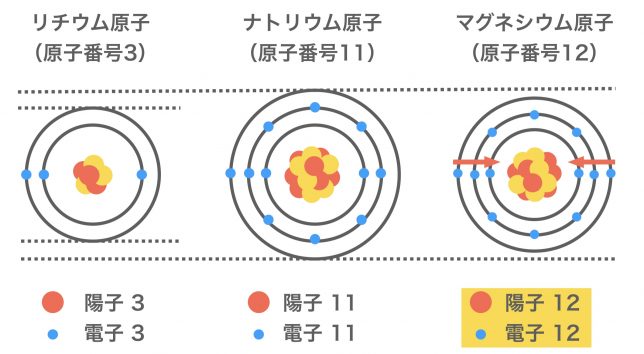
そういうことだね。
マグネシウム原子の方が、外側の電子が中心に引っ張られて、原子が小さくなるんだ。
ということは、⑵の答えは、ナトリウムの方が大きい。ということですね。
それでいいよ。
実際の原子は、ナトリウム原子の半径が0.186nm(ナノメートル)でカリウム原子の半径が0.160nmくらいだよ。
典型元素(1〜2、13〜18族)の第3周期までまとめるとこんな感じだね。
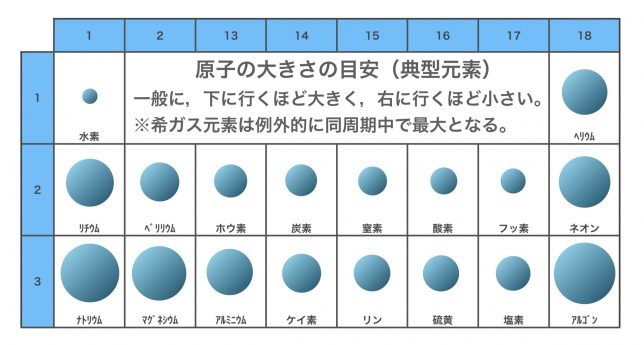
18族の貴ガス元素は、大きくなってますね。
貴ガス元素は例外として、原子半径が同周期中で1番大きくなるよ。
同族・同周期以外の比較
同族や同周期での大小関係についてはわかりました。それ以外の比較はどうするんですか?
どういうことだい?
例えば、ナトリウム原子とカルシウム原子のように、同族でもなければ同周期でもない原子同士の大小関係の比較です。
なるほど、それを答えるのはかなり難しいね。原子番号と原子半径の関係をグラフにするとこうなるよ。
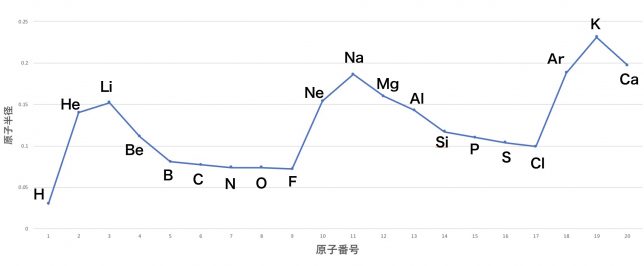
ナトリウム原子と、カルシウム原子だと、わずかにカルシウムの方が大きくなるんですね。
グラフがあればわかるけど、覚えていない限り答えるのは難しいね。ということで、問題として聞かれることはまずないと思っていいよ。ちなみにナトリウム原子の半径は0.186nm、カルシウム原子の半径は0.197nmだよ。
原子の大小比較は、とりあえずは同族と同周期について答えられれば良いということですね。
理由もしっかり答えられるようにね!
✔︎ 原子の大きさは元素によって異なる。
✔︎ 同族では,典型元素は周期表の下ほど大きい。
✔︎ 同周期では,典型元素は周期表の右ほど小さい。
✔︎ 希ガスは同周期中で最大となる。
✔︎ それ以外の比較(斜めでの比較や遷移元素)はしなくて良い。











